Erschienen in:
17.08.2021 | Pankreaskarzinom | Schwerpunkt: Pankreaspathologie
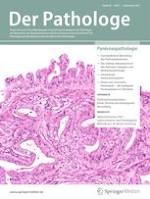
Das duktale Adenokarzinom des Pankreas: Subtypen und Molekularpathologie
verfasst von:
PD Dr. Anna Melissa Schlitter, Björn Konukiewitz, Atsuko Kasajima, Maximilian Reichert, Günter Klöppel
Erschienen in:
Die Pathologie
|
Ausgabe 5/2021
Einloggen, um Zugang zu erhalten
Zusammenfassung
Das duktale Adenokarzinom ist der dominierende Tumor im Pankreas. Obwohl relativ selten, gehört er wegen seiner schlechten, bislang nur wenig verbesserten Prognose zu den großen onkologischen Problemen. Fortschritte gab es in der präzisierten Klassifikation und der standardisierten morphologischen Begutachtung. In der aktuellen WHO-Klassifikation werden die seltenen, prognostisch relevanten Subtypen wie das hochmaligne adenosquamöse Karzinom oder das niedrigmaligne Kolloidkarzinom deutlich untereinander und vom duktalen Adenokarzinom, NOS, abgegrenzt. In der TNM-Klassifikation wurde eine größenbasierte T‑Kategorie eingeführt. Diagnostisch bereitet die histologische Begutachtung am Resektat wenig Probleme. Am Feinnadelpunktat aus dem Primarius oder einer Lebermetastase ist sie jedoch nach wie vor schwierig. Große Fortschritte hat die molekularpathologische Stratifizierung des duktalen Adenokarzinoms und der übrigen Pankreasneoplasien gemacht, wodurch nicht nur die Tumorentitäten genetisch definiert, sondern auch prognoserelevante Tumorgruppen anhand ihrer RNA-Expressionsmuster identifiziert wurden. Das Behandlungsspektrum konnte durch zielgerichtete molekulare Therapien erweitert werden (insbesondere für Patienten mit BRCA1/2-Keimbahnmutationen, NTRK- oder NRG1-Fusionen, onkogenen BRAF- und PIK3CA-Mutationen sowie mit Mikrosatelliteninstabilität [MSI] im Tumorgewebe), auch wenn diese aktuell nur wenigen Patienten (<10 %) zur Verfügung stehen.