Epidemiologie und Lokalisation
Chordome treten jährlich mit einer Inzidenz von 0,08 pro 100.000 Personen auf. Sie wachsen destruierend und sind zum Diagnosezeitpunkt meist schon aus dem Knochen ausgebrochen. Am häufigsten werden sie in der sakrococcygealen Region diagnostiziert (50 %), gefolgt vom Clivus (30 %) und den mobilen Anteilen der Wirbelsäule (20 %) [
5,
30]. Inwieweit biologische Unterschiede zwischen Chordomen verschiedener Regionen (beispielsweise zwischen clivalen und sakralen Chordomen) bestehen, ist derzeit Gegenstand von Untersuchungen [
15]. Chondroide Chordome findet man beinahe ausschließlich im Bereich der Schädelbasis [
23]. Dedifferenzierte Chordome treten am häufigsten im Bereich des Sakrums auf. Niedrig differenzierte Chordome bevorzugen die Schädelbasis und die zervikalen Wirbelkörper [
29]. Speziell bei Chordomen des Erwachsenenalters besteht eine männliche Prädominanz [
26]. Chordome können in jedem Lebensalter auftreten, das mittlere Alter bei Erstdiagnose liegt jedoch bei 58 Jahren [
30]. Pädiatrische Fälle von Chordomen stellen weniger als 5 % dar; diese Tumoren treten bei Kindern typischerweise an der Schädelbasis auf. Wenngleich Chordome sporadische Erkrankungen darstellen, ist in seltenen Fällen eine familiäre Häufung zu beobachten, welche einen autosomal-dominanten Erbgang vermuten lässt [
11]. Darüber hinaus besteht eine bekannte, aber seltene Assoziation mit dem tuberösen Sklerosekomplex (TSC), wobei TSC-assoziierte Chordome praktisch ausschließlich bei Kindern beobachtet werden [
11].
Histologie
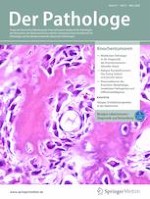
Konventionelles Chordom (Abb.
1c–h): Die Architektur ist typischerweise lobuliert (Abb.
1d). Nekrosen sind vorhanden und können großflächig auftreten. Der Tumor zeigt ein infiltratives Wachstum und umschließt präexistente Knochentrabekel (Abb.
1c, d). Das Tumorgewebe weist eine deutliche extrazelluläre myxoide Matrix auf (Abb.
1f) [
11]. Innerhalb der myxoiden Matrix finden sich große Tumorzellen, in der Regel mit epitheloider Morphologie, die in Nestern und Strängen oder soliden Verbänden gelagert sind (Abb.
1e, f). Diese Tumoren zeichnen sich durch große, polygonale Zellen mit reichlich klarem bis eosinophilem Zytoplasma aus (sog. physaliphore Zellen); darüber hinaus enthalten sie charakteristische, intrazytoplasmatische, blasige Vakuolen (Abb.
1e, f). Die Zellkerne können nukleäre Atypien aufweisen, selten finden sich Mitosefiguren. Wiederkehrende konventionelle Chordome zeigen eine vermehrte Zellularität, vermehrt Atypien und können auch dedifferenzieren.
Chondroides Chordom (Abb.
3a, b): Neben Arealen, die einem konventionellen Chordom entsprechen, finden sich Areale, welche an ein Low-grade-Chondrosarkom (hyaliner Typ) erinnern. Die chondroiden Areale zeigen neoplastische Zellen, die von hyaliner knorpelartiger Substanz umgeben werden (Abb.
3a; [
23]). Im Gegensatz zu kartilaginären Tumoren exprimieren chondroide Chordome jedoch Brachyury (Abb.
3b) und Keratine [
11]. An kleinen Biopsien (in denen konventionelle Chordomareale nicht mitgetroffen sind) ist die Differenzialdiagnose schwierig. Man sollte speziell an der Schädelbasis bei einem Tumor mit chondroid imponierender Grundsubstanz differenzialdiagnostisch immer an ein chondroides Chordom denken. Die Prognose für chondroide und konventionelle Chordome unterscheidet sich nicht.
Dedifferenzierte Chordome machen weniger als 10 % aller Chordome aus [
30]. Sie bestehen aus einer konventionellen Chordomkomponente, die abrupt in ein undifferenziertes pleomorphes Tumorgewebe (in der Regel ein undifferenziertes pleomorphes Sarkom „high-grade not otherwise specified“ [NOS]) übergeht. In seltenen Fällen wurde auch eine osteo-, chondro- oder rhabdomyosarkomatöse Differenzierung beobachtet [
18]. Die Immunreaktivität für Brachyury, Keratine, EMA und S‑100 kann in der dedifferenzierten Tumorkomponente verloren gehen (Abb.
3e). Im Gegensatz zu den niedrig differenzierten Chordomen zeigen sie eine erhaltene INI1-Expression (Abb.
3f). Bei dedifferenzierten Chordomen handelt es sich um den aggressivsten Subtyp. Dedifferenzierte Chordome haben daher eine deutlich schlechtere Prognose als konventionelle und chondroide Chordome [
5,
11,
30].
Niedrig differenzierte Chordome (Abb.
3c, d): Diese Subgruppe der Chordome wurde in den letzten Jahren als sehr seltene Subgruppe beschrieben [
13,
29]. Tumoren bestehen aus kohäsiven Verbänden von epitheloiden Zellen, die in soliden Verbänden wachsen (Abb.
3c). Die Tumorzellen weisen deutliche nukleäre Atypien auf, wenngleich sie Brachyury deutlich exprimieren (Abb.
3d). Typischerweise werden die Tumorzellen von reichlich eosinophilem Zytoplasma umgeben. Auch sind Zellen mit „rhabdoider“ Morphologie beschrieben. Die im klassischen Chordom vorhandenen typischen physaliphoren Zellen treten nicht auf. Auch das typische extrazelluläre myxoide Stroma findet man in diesen Tumoren nicht. Die Tumoren imponieren generell als epitheloide, hochmaligne Neoplasien. Niedrig-differenzierte Chordome entstehen nicht aus einem präexistenten klassischen Chordom.
Molekularpathologie
Es ist derzeit keine definierte genetische Ursache für die Entwicklung und das Wachstum von Chordomen bekannt [
35]. Chordome zeigen üblicherweise einen annähernd diploiden oder moderat haploiden Karyotyp mit etlichen numerischen und strukturellen Rearrangements [
11]. In einigen Fällen werden gehäufte Rearrangements beobachtet, welche im Zuge einer einzigen zellulären Katastrophe simultan auftreten. Dieser Umstand wurde von Stephens et al. als „Chromotripsis“ definiert [
21,
34]. Gröschel et al. sehen eine gestörte homologe Rekombination, einen Mechanismus der zelleigenen Reparatur von DNA-Schäden, als Ursache für eine genetische Instabilität bei fortgeschrittenen Chordomen an [
12]. Ein Verlust von Tumorsuppressorgenen, wie beispielsweise „
breast cancer 2, early onset“ (
BRCA2), als Ursache derartiger genetischer Signaturen konnte von den Autorinnen und Autoren in 3 von 11 Tumoren nachgewiesen werden [
12].
Der homo- oder heterozygote Verlust von „
cyclin-dependent kinase inhibitor 2A“ (
CDKN2A) ist eine bei Chordomen häufig zu beobachtende chromosomale Veränderung.
CDKN2A-Verluste sind jedoch auch bei vielen anderen Tumorentitäten beschrieben und damit nicht chordomspezifisch [
3,
21,
35].
CDKN2A ist ein Tumorsuppressorgen, das für 2 Proteine, p16 und p14ARF, codiert. Das Protein p16 spielt eine funktionelle Rolle in der Regulation des Zellzyklus über cyclinabhängige Kinasen (CDK) und Cyclin D, p14ARF aktiviert den Tumorsuppressor TP53 [
3].
Eine Sequenzierungsstudie an 104 Chordomen zeigte ein vergleichsweise ruhiges Genom dieser Tumoren [
35]. Nur wenige Gene waren mutiert bzw. von genetischen Veränderungen betroffen und mehr als die Hälfte der untersuchten Tumoren ließ jeglichen genetischen Driver vermissen [
35]. Dennoch konnten Duplikationen von
TBXT (27 %) und wiederkehrende Verluste von
CDKN2A auch in dieser Kohorte bestätigt werden [
35]. Gene, welche sich darüber hinaus als vergleichsweise häufig alteriert erwiesen, waren „phosphatidylinositol‑4,5‑bisphosphate 3‑kinase catalytic subunit alpha“ (
PI3KCA, 16 %), Gene des Chromatin-Remodelling-Prozesses (17 %) und das lysosomale Regulatorgen
LYST (10 %). Niedrig differenzierte Chordome zeigen typisch einen Verlust von
SMARCB1/INI1 [
13,
29]. Dabei handelt es sich um ein auf Chromosom 22 lokalisiertes Gen, das in die Art und Weise involviert ist, wie die DNA im Zellkern verpackt wird [
13].
Dem Transkriptionsfaktor Brachyury bzw. dem dafür codierenden Gen
TBXT (6q27) wird neben seiner Rolle als Biomarker für Chordome auch eine Schlüsselfunktion in der Pathogenese dieser Tumoren zugeschrieben [
11,
21,
22,
28,
45]. Duplikationen von
TBXT treten bei familiär gehäuften und bei bis zu 27 % der sporadisch auftretenden Chordome auf [
35,
45]. Eine experimentelle Ausschaltung von
TBXT führte zu einem Wachstumsstopp von Chordommodellen [
21,
22]. Sharifnia et al. konnten basierend auf einem Clustered-regularly-interspaced-short-palindromic-repeats-associated-protein-9(CRISPR/Cas9)-Loss-of-function-Screen die vorhandene Evidenz erhärten, dass
TBXT jenes Gen darstellt, welches für das Überleben von Chordomzellen am essenziellsten ist [
28]. Pillay et al. zeigten, dass ein in der kaukasischen Bevölkerung häufig zu beobachtender Einzelnukleotidpolymorphismus („single nucleotide polymorphism“; SNP) von
TBXT (
rs2305089) hochsignifikant mit dem Risiko für das Auftreten von Chordomen assoziiert ist [
21]. Wenngleich vieles darauf hindeutet, dass
TBXT eine wichtige Rolle in der Entstehung von Chordomen zukommt, ist der detaillierte Pathomechanismus dahinter noch nicht bekannt.
Therapie
Es ist mittlerweise eine allgemein akzeptierte Tatsache, dass die Abklärung und Therapie von Chordomen ein hohes Maß an Spezialisierung erfordert und daher in spezialisierten Referenzzentren erfolgen sollte [
30]. Aktuell stellt die chirurgische En-bloc-Resektion mit negativen Resektionsrändern (R0 gemäß dem Union-for-International-Cancer-Control[UICC]-TNM-Tumorklassifikationssystem) die einzige kurative Behandlungsoption und damit den Goldstandard für die Therapie dieser Erkrankung dar [
5,
30]. Nach R0-Resektionen werden (je nach Fallserie) rezidivfreie 5‑Jahres-Überlebensraten von 50–80 % beschrieben [
5,
30]. R0-Resektionen sind aufgrund der Lokalisation dieser Tumoren jedoch vielfach nicht bzw. nur unter Inkaufnahme schwerer neurologischer Ausfallserscheinungen und anderer Komorbiditäten durchführbar und mit einem hohen Lokalrezidivrisiko vergesellschaftet [
5,
30]. Dies trifft insbesondere auf Tumoren der Schädelbasis bzw. der oberen Halswirbelsäule zu, gilt aber auch für Tumoren, welche sich in den Spinalkanal ausdehnen sowie für sakrale Chordome über dem Niveau von S3. Im Fall von nichtresektablen Tumoren bzw. sofern Patientinnen und Patienten einem operativen Eingriff aufgrund der hohen Morbidität nicht zustimmen, ist die Hochdosisbestrahlung die therapeutische Alternative [
9,
30]. Die vorhandene Evidenz deutet darauf hin, dass eine Bestrahlung mit Protonen und Carbonionen der Photonenbestrahlung von Chordomen physikalisch überlegen ist. Jedenfalls ist sie dies in Hinblick auf eine Dosisreduktion und damit Schonung des umgebenden Gewebes, da Protonen und Schwerionen sich gezielter auf das Tumorvolumen fokussieren lassen [
5,
9]. Da Chordome jedoch generell wenig strahlensensibel sind, ist eine vergleichsweise hohe Dosis von mindestens 74 GyE erforderlich [
5]. Es konnte an kleineren Kollektiven gezeigt werden, dass mit einer Hochdosisbestrahlung von Chordomen lokale Tumorkontrollraten nach 5 und 10 Jahren erzielt werden können, welche mit jenen nach einer adäquaten chirurgischen Versorgung vergleichbar sind [
1,
6,
9,
37]. Aktuell existieren hierzu jedoch noch keine prospektiven und randomisierten Studien. Um künftig ausreichend evidenzbasierte Empfehlungen zur Therapieentscheidung aussprechen zu können, wurde seitens der italienischen Sarkomgruppe in Kollaboration mit einer international agierenden Plattform für Patientinnen und Patienten mit Chordomen (Chordoma Foundation, Durham, NC, USA) eine prospektive, multizentrische klinische Studie initiiert, welche das rezidivfreie Überleben nach definitiver Hochdosisbestrahlung mit jenem nach operativer Versorgung bei Chordompatientinnen und -patienten vergleicht.
Medikamentöse Therapie oder der unerfüllte Bedarf nach neuen Behandlungsoptionen
Aktuell sind keine Medikamente für die Therapie von Chordomen zugelassen [
5,
30]. Zytotoxische Chemotherapien haben sich bei dieser Entität im Allgemeinen als wirkungslos erwiesen, wenngleich einzelne Fallberichte ein Ansprechen von dedifferenzierten und pädiatrischen Chordomen beschreiben [
5,
30]. In der Ära der Präzisionsmedizin ist die Suche nach alternativen therapeutischen Zielstrukturen, welche die Verabreichung „maßgeschneiderter Therapieformen“ im Rahmen von personalisierten Tumortherapien erlaubt, ein zentrales Thema. Bis heute konnten weder einheitliche (epi-)genetische Ursachen für die Entwicklung und das Wachstum von Chordomen identifiziert werden, noch konnten trotz der durch viele Studien belegten essenziellen Bedeutung des Transkriptionsfaktors Brachyury für die Chordomentstehung Durchbrüche in der Entwicklung von maßgeschneiderten Therapien zur Ausschaltung desselben erzielt werden [
28,
35]. Gegen Brachyury gerichtete Immuntherapien zeigten bisher nur mäßige Erfolge [
14], wenngleich aktuell weitere klinische Studien zu immuntherapeutischen Ansätzen, insbesondere in Kombination mit einer Bestrahlungstherapie, durchgeführt werden.
Aufgrund des vergleichsweise häufig beobachteten Verlustes von
CDKN2A mit einem konsekutiven Verlust des Zellzyklusregulators p16 und daraus resultierender Aktivierung des cyclinabhängigen CDK4/6-Pathways wurde basierend auf den Vorarbeiten von Witzleben et al. in Deutschland eine klinische Studie mit dem CDK4/6-Inhibitor Palbociclib (Ibrance®, Pfizer, New York City, NY, USA) initiiert, welche die Wirkung dieses Medikaments an Patientinnen und Patienten mit lokal fortgeschrittenen und metastasierenden Chordomen untersucht [
38]. Auch Sharifnia et al. identifizierten CDK-Inhibitoren, speziell Inhibitoren der Subtypen CDK7/12/13 und CDK9, als potenzielle therapeutische Targets bei Chordomen, wenngleich klinische Daten hierzu noch fehlen [
28]. Eine weitere Multicenter-Phase-II-Studie evaluiert derzeit die Behandlung mit Tazemetostat, einem Inhibitor der Histon-Lysin-N-Methyltransferase „enhancer of zeste 2 polycomb repressive complex 2 subunit“ (EZH2), bei Patientinnen und Patienten mit niedrig differenzierten Chordomen, welche einen Verlust von
SMARCB1/INI1 aufweisen.
Basierend auf ihren Untersuchungen zu gestörten homologen Rekombinationsmechanismen in Chordomen diskutieren Gröschel et al., dass diese Tumoren einer Therapie mit Inhibitoren von Poly(Adenosindiphosphat-Ribose)-Polymerase (PARP) zugänglich sein könnten, da insbesondere Zellen mit gestörten homologen Rekombinationsmechanismen eine Vulnerabilität für diese Gruppe von Inhibitoren aufweisen [
12]. Klinische Studien dazu existieren derzeit jedoch nicht.
In Anbetracht der Tatsache, dass die Analyse genetischer und epigenetischer Veränderungen bisher nicht zur Entdeckung einheitlicher, medikamentös angreifbarer Zielstrukturen bei Chordomen geführt hat, wurde durch unterschiedliche Arbeitsgruppen eine Vielzahl weiterer potenzieller Zielstrukturen evaluiert, von denen bekannt ist, dass sie in die Entstehung anderer Tumorentitäten involviert sind. Dazu zählen diverse Zelloberflächenrezeptoren, Elemente intrazellulärer Signalwege, Zellzyklusregulatoren, immuntherapeutische Marker und andere mehr [
14,
16,
27,
38]. Als Folge dessen existieren kleinere, nichtrandomisierte Studien bzw. Fallberichte zur Behandlungen von Chordomen mit unterschiedlichen kleinmolekularen Tyrosinkinase-Inhibitoren (TKI) [
5,
16,
30]. So zeigte eine nichtrandomisierte klinische Phase-II-Studie mit Imatinib-Mesylat (Glivec®/Gleevec®, Novartis Pharma AG, Basel, Schweiz) ein moderates Ansprechen von Chordomen auf diese Therapie [
5,
30,
32]. Weitere Phase-II-Studien untersuchten Imatinib in Kombination mit den Mammalian-target-of-rapamycin(mTOR)-Inhibitoren Sirolimus (Rapamune®, Pfizer, New York City, NY, USA) [
31] und Everolimus (Afinitor®, Novartis) [
33] ebenfalls mit einem bestenfalls moderaten Ansprechen [
31,
33]. Ein solches wurde auch in zwei weiteren, nichtrandomisierten Studien mit den antiangiogenetisch wirksamen Multikinaseinhibitoren Sunitinib (Sutent®, Pfizer, New York City, NY, USA) [
30] und Sorafenib (Nexavar®, Bayer AG, Leverkusen, Deutschland und Onxy Pharmaceuticals, South San Francisco, CA, USA) beobachtet [
2,
5].
Ergänzend zu hypothesengeleiteten Vorgehensweisen, welche auf vorab definierte Strukturen eines Tumors abzielen, führten einige Gruppen phänotypische Medikamententestungen durch [
17,
25,
28]. Phänotypische Ansätze sind empirisch und testen eine breite Palette an unterschiedlichen Substanzen an einer Vielzahl von Erkrankungsmodellen, ohne eine vorab definierte Hypothese über die Art der potenziellen Zielstruktur und damit auch den erwarteten Wirkmechanismus zu besitzen. Diese Testungen zeigten übereinstimmend, dass die gegen den epidermalen Wachstumsfaktor-Rezeptor („epidermal growth factor receptor“, EGFR) gerichteten Wirkstoffe die beste inhibitorische Wirkung auf das Wachstum von Chordommodellen besaßen, wenngleich auch Resistenzen zu beobachten waren [
17,
25,
28]. Eine EGFR-Expression von klinischen Chordomproben ist nachweisbar [
27] und klinische Fallberichte sowie kleinere Fallserien zeigten positive Effekte unter Therapie mit EGFR-Inhibitoren [
16]. Basierend auf diesen vielversprechenden kollektiven Daten wird aktuell ein EGFR-Inhibitor der zweiten Generation, Afatinib (Gilotrif®, Boehringer Ingelheim, Deutschland), im Rahmen einer europäischen randomisierten Multizenterstudie bei EGFR-exprimierenden Chordomen untersucht [
17]. Es ist derzeit jedoch noch kein zugrunde liegender Mechanismus bekannt, welcher das Ansprechen von Chordomen auf EGFR-Inhibitoren erklären kann. Wenngleich „copy number gains“ (CNGs) der
EGFR-Region vorzuliegen scheinen, konnten diverse Studien keine Amplifikationen oder Mutationen von
EGFR oder verwandten Rezeptoren der ErbB-Familie nachweisen [
17,
25,
28,
35]. Abgesehen von vereinzelten Mutationen von
PI3KCA bzw. Verlusten von „phosphatase and tensin homolog“ (
PTEN) sind auch keine genetischen Veränderungen der nachgeschalteten Signalwege beschrieben [
35]. Der an EGFR bindende und diesen stimulierende epidermale Wachstumsfaktor (EGF) stellt jedoch eine direkte Zielstruktur von Brachyury dar [
20]. D’Agati et al. zeigten darüber hinaus an einem etablierten Zebrafisch-Chordom-Modell [
4], dass eine künstlich herbeigeführte Überexpression der Rezeptortyrosinkinasen (RTK) EGFR und „vascular endothelial growth factor receptor 2“(VEGFR2) die Entstehung von notochordalen Tumoren in diesem Tiermodell zur Folge hatte. Demgegenüber reichte eine vermehrte Expression von
TBXT dazu nicht aus [
8]. Die Autoren folgerten daraus, dass ein mehrstufiger Mechanismus für die Chordomentstehung verantwortlich sein könnte. Auf Basis einer
TBXT-Aktivierung, welche für die Aufrechterhaltung einer notochordalen Differenzierung sorgt, triggert möglicherweise erst die vermehrte Aktivität gewisser
RTK-Gene das eigentliche Tumorwachstum [
8]. Die Frage, inwieweit diese Daten auf den Menschen übertragbar sind bzw. welche Faktoren die entsprechenden Gene beim Menschen gegebenenfalls aktivieren, kann diese Arbeit alleine jedoch nicht beantworten [
8]. Ergebnisse von klinischen Studien, welche abgesehen von einer Evaluierung des therapeutischen Effektes auch weitere Biomarker generieren sollen, bleiben somit abzuwarten.